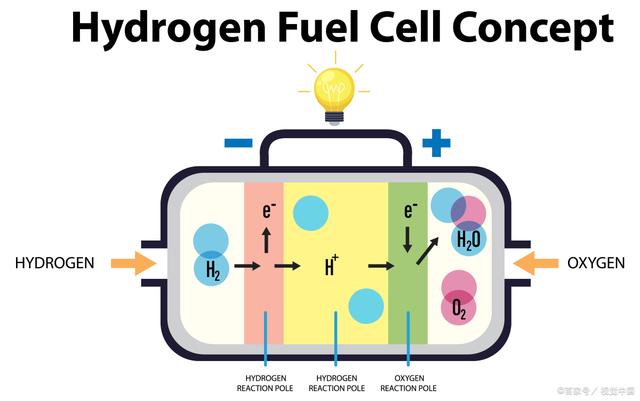
氢燃料电池的工作原理
|
氢燃料电池是一种将氢气作为燃料,通过化学反应产生电能的装置。相比传统燃烧燃料的方法,氢燃料电池有着更高的能源转化效率和更低的排放,成为未来环保能源的重要技术之一。本文将介绍氢燃料电池的工作原理。 电化学反应 氢燃料电池的基本原理是利用氢气和氧气在电极上发生氧化还原反应,从而产生电能。该反应式如下: 2H2 O2 → 2H2O 2e- 其中,氢气在阳极上被氧化成离子和电子,而氧气在阴极上被还原成水。离子通过电解质传递到阴极,电子则通过外部电路传递到阳极,形成电流。由于氧化还原反应产生的电位差,电流可以用于驱动外部电路和设备。 电极和电解质 氢燃料电池的电极通常由贵金属制成,如铂、钯和铑。阳极上的贵金属催化剂可以促进氢气的氧化反应,从而产生电子。阴极上的贵金属催化剂可以促进氧气的还原反应,从而接受电子并形成水。电极与电解质之间的物理隔离可以防止氧气和氢气混合产生爆炸。 电解质是一种可离子化的物质,通常是固体聚合物或液体溶液。它们具有良好的离子传递和阻挡电子传输的性能,可以防止电极之间的电子直接传递,同时使离子得以传递到阴极。典型的电解质包括固体聚合物膜和液态电解质溶液。 氢气输入 氢气输入是氢燃料电池工作的重要组成部分。通常,氢气以压力瓶的形式储存,并通过管道输入到阳极。为了确保氢气输入的纯度和质量,通常需要使用氢气净化系统。氢气净化系统可以通过去除杂质和不纯物质,提高氢气的纯度和质量,从而确保电池的正常运行。 应用前景 氢燃料电池技术具有广泛的应用前景,在能源转化和储存领域具有很高的价值。氢气作为一种清洁、高效的能源,可以广泛应用于交通运输、工业生产、航空航天和家庭能源等领域。氢燃料电池的应用可以降低能源消耗和环境污染,对于实现可持续发展和环保能源的开发具有重要意义。 结论 本文介绍了氢燃料电池的工作原理,包括电化学反应、电极、电解质和氢气输入等关键组成部分。该技术在能源转化和储存领域具有广泛应用前景,可以为环保能源的开发做出贡献。 然而,氢燃料电池技术目前还存在着一些挑战和问题,如氢气储存和输送、电极催化剂的高成本、电解质稳定性等。因此,未来需要进一步研究和开发新的材料和技术,提高氢燃料电池的效率和可靠性,从而实现其广泛应用的商业化和普及。 综上所述,氢燃料电池是一种具有很高应用前景的能源转化和储存技术,其基本原理是利用氢气和氧气在电极上发生氧化还原反应,产生电能。氢燃料电池技术可以为实现可持续发展和环保能源的开发做出贡献,但仍需要进一步研究和开发以解决存在的问题和挑战
|